AMES Test kit
Principio del test
I ceppi tester di Ames sono i ceppi di S. typhimurium ed E. coli che sono stati utilizzati per più di 40 anni per rilevare composti mutageni.
Mutazioni puntiformi sono state effettuate nell’istidina (Salmonella typhimurium) o nell’operone del triptofano (Escherichia coli), rendendo i batteri incapaci di produrre il corrispondente amminoacido. Queste mutazioni danno luogo a -his o -trp organismi che non possono crescere a meno che non vengano forniti istidina o triptofano.
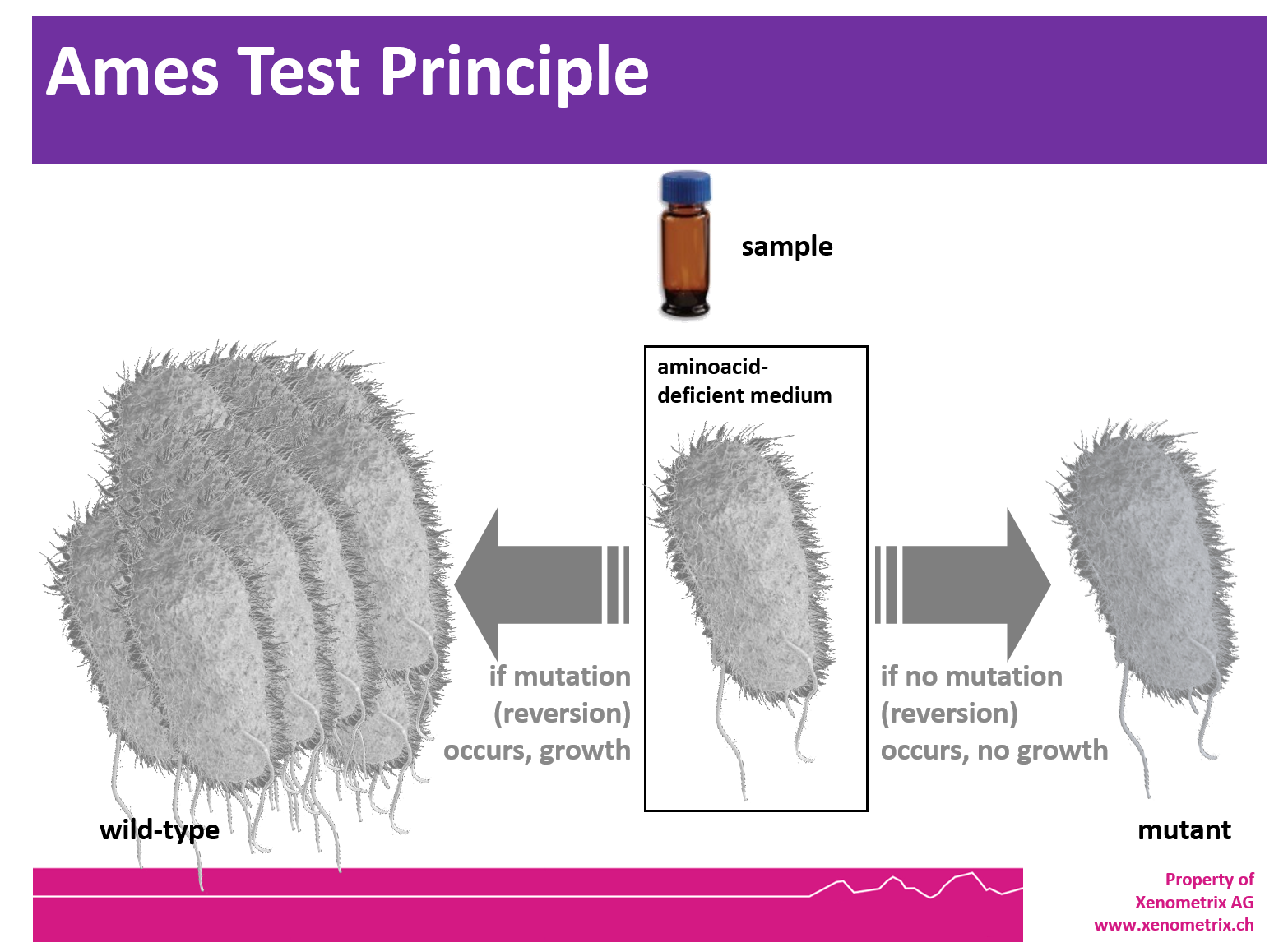
Il potenziale mutageno di un campione di prova viene valutato esponendo questi organismi che richiedono aminoacidi a concentrazioni variabili del campione e selezionando l’evento di reversione. Per questa selezione vengono utilizzati terreni privi di istidina o triptofano che consentono solo a quelle cellule che hanno subito la reversione alla prototrofia istidina / triptofano di sopravvivere e crescere.
Un evento mutageno che causa sostituzioni di basi o mutazioni frameshift all’interno del gene può causare un ritorno alla prototrofia degli amminoacidi. Questi batteri ripristinati cresceranno rispettivamente in terreni carenti di istidina o triptofano, mentre i batteri non ripristinati non saranno in grado di crescere. I terreni durante la fase di crescita possono essere liquidi o a base di agar.
Ames Test su piastre di Agar – OECD 471 – Descrizione
I ceppi congelati appena scongelati vengono inoculati nel terreno di coltura e le colture vengono coltivate durante la notte a 37 ° C in uno shaker ambientale in presenza (TA98, TA100, E. coli WP2 [pKM101], E. coli WP2 uvrA [pKM101]) o assenza (TA1535, TA1537, E. coli WP2 uvrA) di ampicillina. Le colture notturne vengono utilizzate la mattina successiva per il test di incorporazione o preincubazione di Ames.
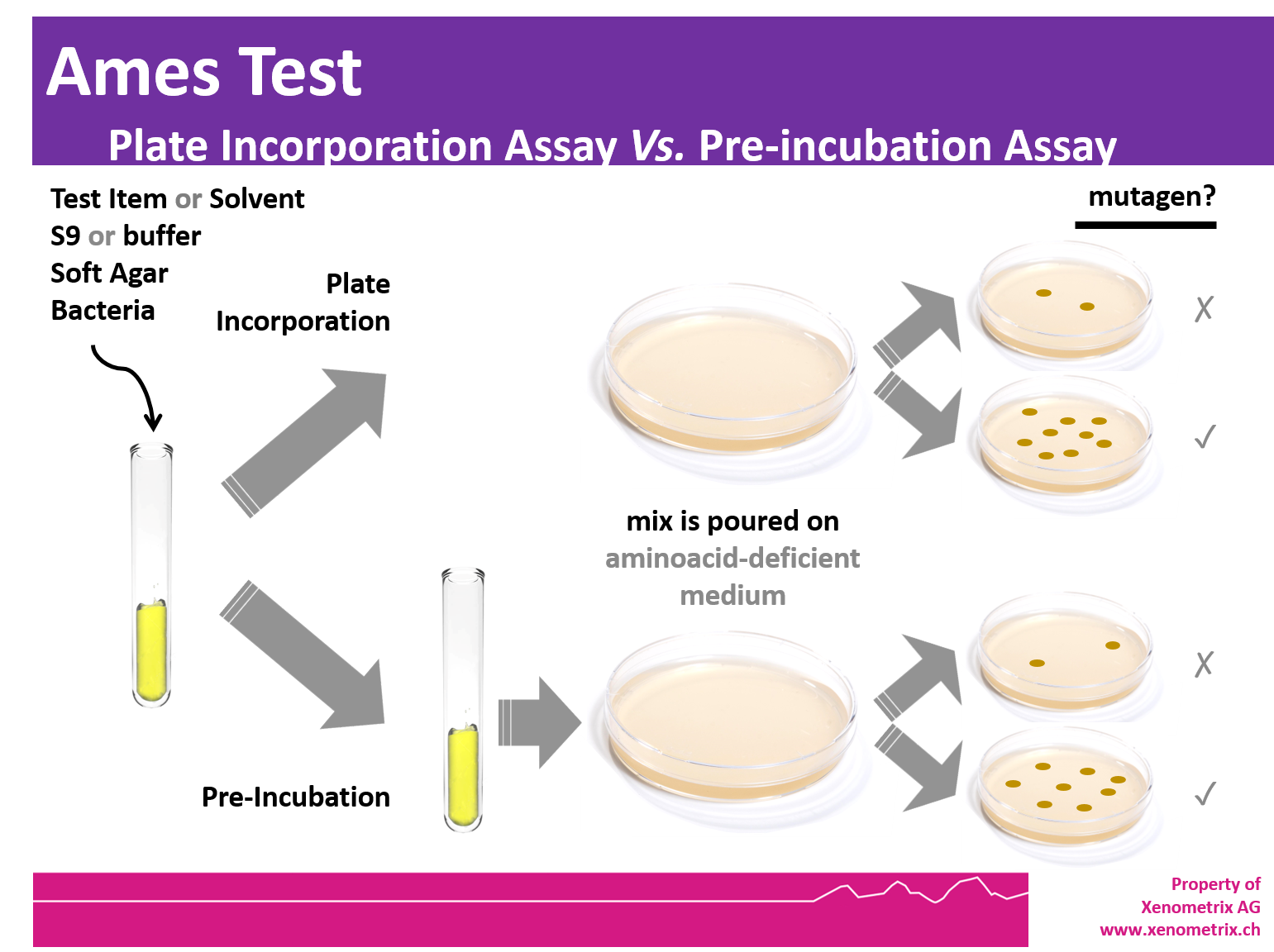
I ceppi tester vengono esposti alla sostanza chimica per 20 min a 37 ° C prima di essere inseriti in su piastre di agar con glucosio minimo. I componenti della miscela di preincubazione sono la miscela S9 o il tampone fosfato, la soluzione chimica in esame e la coltura batterica. Dopo 20 min a 37 ° C, alla miscela viene aggiunto agar top fuso integrato con istidina / biotina o triptofano e mantenuto a 48 ° C. Il contenuto viene miscelato e versato su piastre di agar glucosio minimo. Dopo 48-72 ore a 37 ° C, il numero di colonie per piastra e per dose viene contato a occhio e confrontato con il numero di colonie spontanee revertanti ottenute nelle piastre di controllo negativo. Le linee guida relative al test di Ames sono OECD 471, ICH M7.
Ames Test MPF – Liquid Microplate Fluctuation Ames Test OECD 471, ICH M7 – Descrizione del saggio
La crescita durante la notte è identica alla procedura descritta in precedenza (Test di Ames su piastre di agar – Descrizione del saggio).
I batteri vengono esposti a 6 concentrazioni di un campione di prova, nonché un controllo positivo e uno negativo, per 90 minuti in un mezzo contenente una quantità sufficiente di istidina (S. typhimurium) o triptofano (E. coli) per supportare circa due divisioni cellulari. Dopo l’esposizione, le colture in ciascuna condizione (controllo negativo, campioni di test e controlli positivi) vengono diluite in un mezzo indicatore di pH privo di istidina o triptofano e aliquotate in 48 pozzetti di una piastra da 384 pozzetti.
Entro due giorni, le cellule che hanno subito il ritorno alla prototrofia degli amminoacidi cresceranno. Nel sistema liquido Ames II / Ames MPF, il metabolismo batterico riduce il pH del terreno, cambiando il colore del pozzetto in cui si trovano i batteri. Il numero di pozzetti contenenti colonie revertanti viene contato per ciascuna dose e confrontato con un solvente (negativo) di controllo. Ogni dose viene testata in triplicato per consentire l’analisi statistica dei dati.
Un aumento dose-dipendente e il significativo del numero di colonie revertenti all’esposizione al campione di prova rispetto ai controlli con solvente indica che il campione è mutageno.
Il potenziale mutageno dei campioni viene valutato direttamente e in presenza di attivazione metabolica, fornita dal fegato di ratto liofilizzato, S9.
Linee guida per il test di Ames: OECD 471, ICH M7.
Ames MPF Test™ step-by-step
Questo video mostra come eseguire il test di Ames MPF ™ o Ames II passo a passo aiutandovi a configurare il dosaggio. Mostra anche tutti gli strumenti e il materiale necessari per eseguire il saggio Ames MPF ™ o Ames II.
https://youtu.be/-nwsyLBwjaY
Kit pronti all’uso o singoli prodotti?
Kit pronti all’uso, inclusi ceppi, media, ampicillina, S9, controlli positivi sono disponibili nell’ Ames MPF, così come in formato piastre agar a 6 o 24 pozzetti.
I kit pronti all’uso sono di qualità controllata dal fenotipo dei ceppi, dai controlli positivi e dalla frazione microsomica del fegato di ratto S9 e quindi sono un sistema più standardizzato. Gli studi di stabilità, il controllo della crescita, gli studi di tossicità dell’ S9 e i controlli positivi sono eseguiti in modo continuo.
Ulteriori informazioni:
• Ames Tester Strains
• Rat liver S9
Leggi qui uno studio di stabilità dei ceppi Ames Tester
191105_02_Stability_Ames_Tester_Strains
